المحتوى
- العثور على إلكترونات التكافؤ لجميع العناصر باستثناء المعادن الانتقالية
- العثور على إلكترونات التكافؤ للمعادن الانتقالية
- نصائح
تدور الإلكترونات حول نواة الذرة عند مستويات طاقة محددة تعرف باسم مستويات الطاقة الرئيسية ، أو قذائف الإلكترون. كل غلاف إلكترون يتكون من قشرة فرعية واحدة أو أكثر. بحكم التعريف ، تنتقل إلكترونات التكافؤ في المنطقة السفلية البعيدة عن نواة الذرة. تميل الذرات إلى قبول أو فقدان الإلكترونات إذا كان ذلك سيؤدي إلى قشرة خارجية كاملة. وفقا لذلك ، تؤثر إلكترونات التكافؤ بشكل مباشر على كيفية تصرف العناصر في تفاعل كيميائي.
العثور على إلكترونات التكافؤ لجميع العناصر باستثناء المعادن الانتقالية
تحديد موقع العنصر المطلوب في الجدول الدوري. يحتوي كل مربع على الجدول الدوري على رمز الحرف لعنصر ed مباشرة أسفل الرقم الذري للعنصر.
على سبيل المثال ، حدد موقع عنصر الأكسجين في الجدول. يمثل الأكسجين بالرمز "O" وله عدد ذري 8.
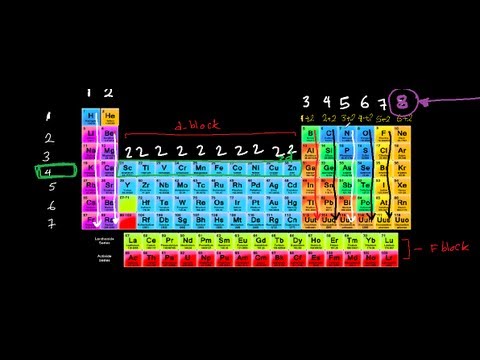
حدد رقم المجموعة ورقم فترة العنصر. تسمى الأعمدة الرأسية للجدول الدوري ، العد من اليسار إلى اليمين ، من 1 إلى 18 ، مجموعات. في الجدول الدوري ، توجد عناصر لها نفس الخصائص الكيميائية في نفس المجموعة. تسمى الصفوف الأفقية للجدول الدوري ، من 1 إلى 7 ، بالفترات. تتوافق الفترات مع عدد قذائف الإلكترون التي تمتلكها ذرات العناصر الموجودة في هذا الصف.
تم العثور على الأكسجين في الفترة 2 ، المجموعة 16.
قم بتطبيق قاعدة الجدول الدوري على العنصر الخاص بك. القاعدة هي كما يلي: إذا لم يكن العنصر معدنًا انتقاليًا ، تزداد أعداد الإلكترونات التكافؤية أثناء عد المجموعات من اليسار إلى اليمين ، على مدار فترة. تبدأ كل فترة جديدة بإلكترون واحد التكافؤ. استبعد المجموعات من 3 إلى 12. هذه معادن انتقالية لها ظروف خاصة.
باتباع هذه القاعدة: تحتوي العناصر الموجودة في المجموعة 1 على إلكترون واحد للتكافؤ ؛ العناصر الموجودة في المجموعة 2 لها إلكترونان متساويان ؛ العناصر في المجموعة 13 لها ثلاثة إلكترونات التكافؤ ؛ العناصر في المجموعة 14 لها أربعة إلكترونات التكافؤ ؛ وهكذا يصل إلى المجموعة 18. العناصر الموجودة في المجموعة 18 بها ثمانية إلكترونات التكافؤ ، باستثناء الهيليوم ، الذي يحتوي على اثنين فقط.
يقع الأكسجين في المجموعة 16 على الجدول الدوري ، لذلك لديه ستة إلكترونات التكافؤ.
