المحتوى
المليغرام ، مختصر ملغ ، عبارة عن وحدة متريّة من الكتلة أو الوزن تُعرف بأنها ألف من الجرام. الميلي فولي هو مقياس لكمية الأيونات في سائل المنحل بالكهرباء. جزء واحد من الألف واحد من الألف من شحنة الشحن ويمثله الرمز mEq. تختلف أيونات العناصر المختلفة في الكتلة ، لذلك من الضروري معرفة الوزن الذري أو الجزيئي للأيونات وتكافؤها قبل حساب التحويل.
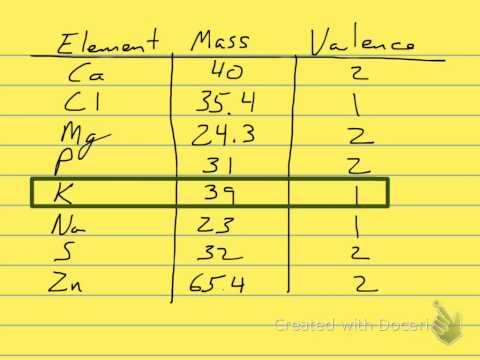
حدد تكافؤ الأيونات ذات الصلة من خلال الرجوع إلى جدول قيم التكافؤ. اضرب هذه القيمة بالكتلة المعبر عنها بالملليغرام. على سبيل المثال ، 20 ملغ من Al +++، الذي يحتوي على تكافؤ ثلاثة ، ينتج نتيجة 60: 3 × 20 = 60.
ابحث عن الكتلة الذرية أو الجزيئية للأيونات ، ثم قسّمها على النتيجة من الخطوة السابقة. والنتيجة هي القيمة الأيونية للأيونات.
الألومنيوم ، المستخدم في المثال السابق ، عنصر نقي ، لذا أنشئ كتلته الذرية. هذا هو 27. التكافؤ مضروب في مثال الكتلة هو 60 ، لذلك قسّم 27 على 60. والنتيجة ، 0.45 هي القيمة الفصلية للكتلة النموذجية.
تحقق من وجود أخطاء عن طريق عكس الحسابات. قسّم قيمة mEq على الكتلة الذرية أو الجزيئية مضروبة في التكافؤ. إذا لم تكن النتيجة الكتلة الأصلية بالملغ ، فقد حدث خطأ في حساباتك. كررها حتى تكون الإجابة صحيحة.