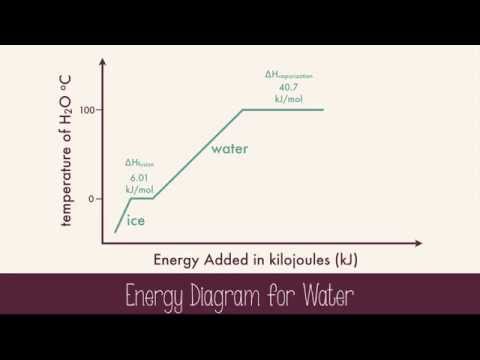
الحرارة المولية للتبخير هي الطاقة اللازمة لتبخير أحد الخلد من السائل. الوحدات عادة ما تكون كيلوجول لكل مول ، أو كيلو جول / مول. يمكن أن تساعدك معادلتان ممكنتان على تحديد الحرارة المولية للتبخير. لحساب حرارة التبخير المولي ، اكتب معلوماتك المعينة ، واختر معادلة تناسب الظروف ، ثم حل المعادلة باستخدام بيانات الضغط ودرجة الحرارة المعطاة.
اكتب معلوماتك المقدمة. من أجل حساب الحرارة المولية للتبخير ، يجب عليك كتابة المعلومات التي توفرها المشكلة. ستوفر المشكلة إما ضغطين وقيمتي درجة حرارة ، أو الحرارة المولية للتسامي ، والحرارة المولية للانصهار. إن الحرارة المولية للتسامي هي الطاقة اللازمة لتسامي أحد الخلد لمادة صلبة ، والحرارة المولية للانصهار هي الطاقة اللازمة لإذابة أحد الخلد لمادة صلبة.
حدد المعادلة التي يجب استخدامها. عند حساب حرارة التبخير المولي ، عليك أن تقرر المعادلة التي ستستخدمها بناءً على المعلومات المقدمة. إذا كانت المشكلة توفر اثنين من الضغط وقيم درجة الحرارة ، استخدم المعادلة ln (P1 / P2) = (Hvap / R) (T1-T2 / T1xT2) ، حيث P1 و P2 هما قيم الضغط ؛ Hvap هي الحرارة المولية للتبخير. R هو ثابت الغاز ؛ و T1 و T2 هي قيم درجة الحرارة. إذا كانت المشكلة توفر الحرارة المولية للتسامي والحرارة المولية للانصهار ، فاستخدم المعادلة Hsub = Hfus + Hvap ، حيث Hsub هي الحرارة المولية للتسامي و Hfus هي الحرارة المولية للانصهار.
حل المعادلة. إذا كنت تستخدم المعادلة ln (P1 / P2) = (Hvap / R) (T1-T2 / T1xT2) ؛ قيمة ثابت الغاز ، R ، هي 8.314 J / Kxmol. على سبيل المثال ، إذا كانت P1 = 402mmHg ، P2 = 600mmHg ، T1 = 200K ، و T2 = 314K ، فإن Hvap تساوي 1834 J / mol. يمكنك بعد ذلك تقسيم إجابتك على 1000 ، نظرًا لوجود 1000 جول في كل كيلوجول. الجواب ثم يصبح 1.834 كيلو جول / مول. إذا كنت تستخدم المعادلة ، Hsub = Hfus + Hvap ، فأنت تطرح Hfus من Hsub. على سبيل المثال ، إذا كان Hsub = 20 kJ / mol ، و Hfus = 13 kJ / mol ، فإن Hvap = 7 kJ / mol.