المحتوى
••• Neznam / iStock / GettyImages
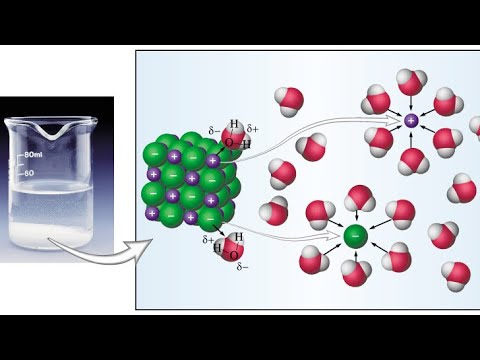
المركبات الأيونية هي تلك المكونة من ذرات مشحونة معاكسة ، تسمى الأيونات ، مرتبة في هيكل شبكي. الأملاح ، بما في ذلك كلوريد الصوديوم (NaCl) - ملح الطعام - هي أفضل الأمثلة المعروفة للمركبات الأيونية. عند غمر مركب أيوني في الماء ، تنجذب الأيونات إلى جزيئات الماء ، كل منها يحمل شحنة قطبية. إذا كان الانجذاب بين الأيونات وجزيئات الماء كبيرًا بما يكفي لكسر الروابط التي تربط الأيونات معًا ، يذوب المركب. عندما يحدث هذا ، تنفصل الأيونات وتتفرق في المحلول ، وتحيط كل منها بجزيئات الماء لمنعها من التوحيد. يصبح المحلول الأيوني الناتج إلكتروليتًا ، مما يعني أنه قادر على توصيل الكهرباء.
هل جميع المركبات الأيونية تذوب؟
بحكم ترتيب ذرات الهيدروجين حول الأكسجين ، يحمل كل جزيء ماء شحنة قطبية. تنجذب نهايتها الإيجابية للأيونات السالبة في مركب أيوني ، في حين تنجذب النهاية السالبة إلى الأيونات الموجبة. يعتمد الميل إلى ذوبان المركب في الماء على قوة الروابط التي تربط المركب معًا مقارنة بالقوة التي تمارسها جزيئات الماء على الأيونات الفردية. تتحلل المركبات شديدة الذوبان ، مثل NaCl ، تمامًا ، بينما تتحلل المركبات التي تحتوي على ذوبان منخفض ، مثل كبريتات الرصاص (PbSO)4) افعل ذلك جزئيًا فقط. المركبات مع الجزيئات غير القطبية لا تذوب.
كيف المركبات الأيونية تذوب
في المحلول ، يعمل كل جزيء ماء مثل المغناطيس الصغير الذي يخلق قوة جذب على الأيونات في المذاب. إذا كانت القوة المشتركة لكل جزيئات الماء المحيطة بالمذاب أكثر من قوة الانجذاب بين الأيونات ، فإن الأيونات تنفصل. كما يفعل كل واحد ، فإنه محاط بجزيئات الماء ، والتي تمنعه من إعادة التوحيد. الأيونات الإيجابية والسلبية تنجرف إلى الحل. عندما تلتصق جميع جزيئات الماء بالأيونات ولم تعد متوفرة ، يُقال إن المحلول مشبع ولن يذوب أكثر من المذاب.
ليست كل المركبات قابلة للذوبان على حد سواء. يذوب البعض جزئيًا فقط لأن تركيز الأيونات في المحلول يصل بسرعة إلى توازن مع المركب غير المنحل. ثابت الذوبان المنتجس يقيس هذه نقطة التوازن. وكلما ارتفع Kس، وارتفاع الذوبان. يمكنك العثور على Kس من مركب معين من خلال البحث عنه في الجداول.
تحول الأيونات الماء إلى المنحل بالكهرباء
يسمح وجود أيونات حرة في الماء للماء بتوصيل الكهرباء ، وهو أمر مهم للكائنات الحية. تحتوي السوائل في جسم الإنسان على أيونات إيجابية مثل الكالسيوم والبوتاسيوم والصوديوم والمغنيسيوم وأيونات سالبة مثل الكلوريد والكربونات والفوسفات. هذه الأيونات هي حيوية للغاية لعملية التمثيل الغذائي بحيث يجب تجديدها عندما يجف الجسم من خلال ممارسة الرياضة أو المرض. هذا هو السبب في أن الرياضيين يفضلون المشروبات كهربائيا على الماء النقي.
حلول التحليل الكهربائي تجعل البطاريات ممكنة. حتى الخلايا الجافة تحتوي على المنحل بالكهرباء ، على الرغم من أنها عجينة بدلاً من سائل. تتدفق الأيونات في المنحل بالكهرباء بين الأنود والكاثود للبطارية ، حيث تشحنها بالنسبة لبعضها البعض. عند توصيل البطارية بالتحميل ، تتدفق المحطات الطرفية وتتدفق الكهرباء.